Prueba in vitro de un paso para la determinación cualitativa
de antígenos para el nuevo coronavirus 2019
(2019-nCoV, SARS-CoV-2)
Prueba rápida basada en inmunocromatografía para la determinación cualitativa de antígenos para el nuevo coronavirus 2019 (2019-nCoV, SARS-CoV-2), con la misma fiabilidad que las PCR y en solo 15 minutos.
Este Test es una herramienta rápida de cribado suplementaria para los portadores sintomáticos o asintomáticos del virus SARS-CoV-2. Requiere de una implantación periódica, conjuntamente con las medidas de higiene.
Información General 2019-nCoV
Los síntomas iniciales de los pacientes son fiebre, fatiga y tos, y gradualmente desarrollan disnea y otra series de manifestaciones graves.
La mayoría de los pacientes tienen una buena prognosis, pero algunos de los casos severos pueden tener el síndrome de dificultad respiratoria aguda, choque séptico o incluso la muerte. Actualmente, no hay un tratamiento específico para la enfermedad.
Conviene recordar que la infección no se detecta inmediatamente tras el contagio, sino que trancurren varios días en periodo de incubación después de que se produzca el contagio por el 2019-nCoV.


Dispositivo médico de diagnóstico in vitro para la detección cualitativa de antígenos de SARS-CoV-2 en muestras de saliva humana y muestras nasofaringeas en 10 minutos
PCL COVID 19 Ag Gold Saliva es un dispositivo médico de diagnóstico in vitro para la detección cualitativa de antígenos de SARS-Cov-2 en muestras de saliva humana y muestras nasofaríngeas en 10 minutos.
Dispositivo médico de diagnóstico in vitro basado en un ensayo inmunocromatográfico para la detección cualitativa de antígeno de SARS- Cov- 2 en muestras humanas de saliva y nasofaríngeas. Esta prueba debe ser empleada en personas sospechosas COVID-19 por personal profesional en el laboratorio o punto de atención.
Cualidades técnicas
En muestras de saliva
- Límite de Detección (LoD): 1.44 x 103 TCID50/ml
- Sensibilidad: 94,29% (IC 95%: 80,84%- 99,30%)
- Especificidad: 100% (IC 95%: 94,87%-100%)
En muestras nasofaríngeas:
- Límite de Detección (LoD): 1.44 x 103 TCID50/ml
- Sensibilidad: 90% (IC 95%: 85,00%- 99,30%)
- Especificidad: 100% (IC 95%: 94,87%-100%)
Manejo del Kit
Diferentes tipos de muestra han sido validadas con PCL COVID19 Ag Gold Saliva.
Muestras de Saliva
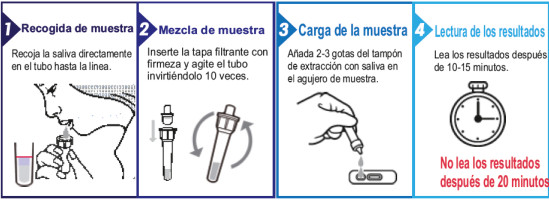
- Recoja la saliva en la punta de la lengua durante 30 segundos (no incluir el esputo). Escupa la saliva en el tubo de tampón de extracción.
- Cubra el tubo con la tapa filtrante y apriete la tapa. Invierta el tubo 10 veces para mezclar la muestra.
- Abra la bolsa y coloque la tira de ensayo en una superficie plana. Deje caer 2-3 gotas en el orificio de la muestra.
- Lea los resultados después de 10 minutos.
Muestras nasofaríngeas
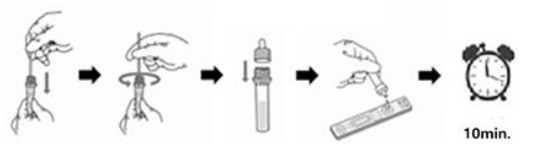
- Inserte el hisopo a través de la fosa nasal y empuje suavemente el hisopo hacia la nasofaringe posterior. Gire el hisopo de muestreo tres veces.
- Ponga el hisopo en el tubo de tampon de extracción.
- Remueva el hisopo 10 veces y luego retírelo mientras exprime el líquido del hisopo.
- Cubra el tubo con la tapa filtrante y mezcle invirtiendo 10 veces.
- Abra la bolsa y coloque la tira de ensayo en una superficie plana. Deje caer 2-3 gotas en el orificio de la muestra.
- Lea los resultados después de 10 minutos.
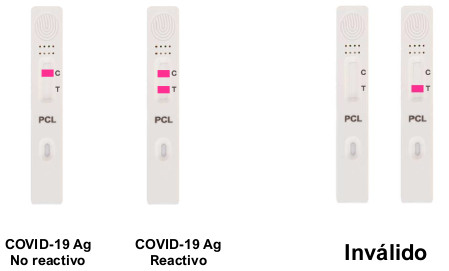
Interpretación de los resultados
El resultado será válido y “no reactivo” cuando solo observe una banda en el lugar de control (C), lo que significa que no se ha detectado antígeno de SARS-Cov-2. Si además observa una segunda banda en el lugar de ensayo (T), el resultado es válido y “reactivo”, lo que significa que se detectaron antígenos de SARS-Cov-2. En caso de no obtener ninguna línea u obtener una única banda en el lugar de ensayo (T), el resultado no es válido y no puede ser utlizado porque la prueba no funcionó como se pretendía.